食品の機能性表示制度で広がるビジネスチャンス②
~“20年先行く”米国ヘルスケア市場の変遷とビジネス事例~前編
2015/04/27
4月1日に食品の機能性表示制度が施行された。44年ぶりの大改定といわれている今回の新制度。その施行によって日本市場はどうなっていくのか。ビジネスチャンスはどのように広がっていくのか。電通ヘルスケアチームのメンバーが有識者に話を聞いた。
日本の食品の機能性表示制度は、米国のダイエタリーサプリメント制度を参考に検討が重ねられてきました。米国で機能性表示が導入されたのが、今から約20年前。それ以降、米国のヘルスケア市場はどう変貌を遂げたのか。また、日本市場との共通点と相違点は何なのか。健康食品のグローバル市場に詳しいグローバルニュートリショングループの武田猛氏に聞いた。

国の関与が最も少ない、米国と日本の機能性表示制度
瀧澤:まず、日本の機能性表示制度が、各国の制度と比較してどのようなポジションにあるのか伺えますか。
武田:食品の機能性表示は、WHO(世界保健機関)とFAO(国連食糧農業機関)が一緒に作った「コーデックス」という国際的なルールがあるのですが、ヘルスクレーム(健康強調表示)は、①栄養素機能強調表示②その他の機能強調表示(米国では「構造/機能強調表示」)③疾病リスク低減表示―の3段階に分かれています。
さらに制度的な側面からは、①国が規格基準をつくる規格基準型②国が個別審査して許可する個別評価型③民間企業が国に届けを出す届け出制―の3タイプに分かれます。その分類に従って、各国の制度を配したのが下の図です。
【図1】
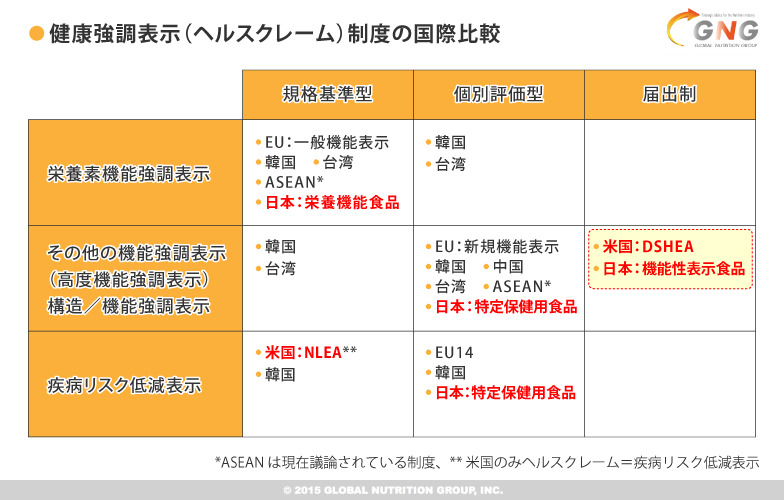
ご覧になって分かるように、米国のダイエタリーサプリメント健康教育法(DSHEA)に基づく制度と、日本の機能性表示制度は、ヘルスクレームにおいては「その他の機能強調表示」、制度的な側面では「届け出制」というポジションになります。国の関与が極めて低い、この2国の届け出制度は、世界的に見れば非常に特異なケースと言っていいでしょう。
健康維持が国家財政に直結することを宣言した米国
瀧澤:米国の制度の重要なポイントは何でしょうか。
武田:米国の制度は、消費者の健康上の利益のために、また国家の医療費削減への貢献のために定められた教育法であると、明確に位置付けられています。単なる表示制度ではなく、消費者を啓発することを制度の理念としているわけですね。
瀧澤:米国での制度成立の背景には、どのような問題意識があったのでしょうか。
武田:法案が連邦議会を通過するときに明示された15項目の付帯事項を見ると、当時の米政府の問題意識や、制度の狙いがよく分かります。主な項目を紹介しますと――。
【図2】
➊米国民の健康状態の改善が合衆国連邦政府の最優先課題である。
➋ある種の栄養成分とダイエタリーサプリメントの摂取は、癌、心臓病、及び骨粗鬆症等の成人病の予防に関連している。また、慢性疾患のいくつかは、野菜、植物由来の食品を中心とした食事で予防可能である。
➌セルフメディケーション、健康に対する知識の向上、十分な栄養摂取、ダイエタリーサプリメントの適切な使用等は、慢性疾患の発症率の低減、介護費削減に貢献する。
➍健康的なライフスタイルは、寿命を延ばすだけではなく、医療費を削減する。医療費削減は、米国の将来にとって最重要課題で、経済的発展の基礎となる。
➎ダイエタリーサプリメントの健康に対する有効性を示す科学研究の情報を知らせ、その知識に基づき消費者が予防的健康管理対策を選択できるようにするべきである。
➏連邦政府は製品の安全性を欠く/品質不良製品には迅速な処置が求められるが、同時に 不合理な制約で、消費者への安全な製品や正確な情報を制約、遅延させてはならない。
武田:施行から4年ほどは前年比13~14%という高い伸長率を維持しました。しかし、1990年代後半と2000年代の前半に急激に落ち込みました。表示詐称など、ルールを守らない企業が続出したことや健康被害が起きたことなどが原因ですが、いくら科学的な根拠に裏付けられた表示をしたとしても、一部の企業の不祥事で、消費者の信用は一気に失われてしまうことを如実に物語っています。また、成長率が鈍化したもう一つの理由に、当時、学術界からサプリメントに対する否定的な論文が幾つか出たことも挙げられます。誇大広告が目立って、それに対して科学者の立場から一石を投じた側面があったのではないかと思います。ただし、そういう事態はあったとしても、制度施行後から近年までのサプリメントの市場規模は一貫して伸びています。年間の平均成長率は8%程度で、日本よりもはるかに高い成長率を20年以上続けています。
米国の制度の成功・失敗に学んだ日本の新制度
瀧澤:米国の機能性表示制度が優れているのはどのような点だとお考えですか?
【図3】

武田:まずGMP(適正製造規範)の準拠を義務付けていることが挙げられます。日本の制度では、GMP制度は企業の任意(努力義務)です。また、FDAが製造工場などに直接監査・査察に行くのも、安全性の確保のためには非常に有効なルールだと思います。
あと、ダイエタリーサプリメントオフィスの設置ですね。これは、国立衛生研究所(NIH)の中に専門のオフィスがあって、サプリメントの有効性や安全性に関して評価しています。年間予算が20億円ほど付いていて、国がこのような取り組みに積極的であることには、非常に大きな意味があると思います。

瀧澤:では、米国の制度が抱える課題は?
武田:製品情報の届け出が販売後30日以内でいいというのは問題でしょうね。それと、製品情報としての機能性表示に根拠情報の提出が必要ないというのも、消費者からすれば不安が残るのではないかと思います。いくら企業の自己責任とはいえ、消費者は、書いてあることをそのまま信用するしかないわけですから。
瀧澤:そのような米国の問題点は、日本の制度では、解決されているのでしょうか。

武田:ご承知のように、根拠となるエビデンス情報は、届け出た内容を消費者庁が公開するので、誰でも見ることができる。それから、米国の場合は、機能性表示の科学的根拠に関する指針が曖昧で強制力を持っていないのですが、日本の場合は消費者庁がきめ細かく手順などを示しています。監視・指導体制が不十分という米国の問題点についても、日本では届け出た情報をネットで公開するという形を取っているので、それがある意味、チェック機能を補う役目も果たします。日本の新制度では、米国の制度の弱点をほぼクリアできているのではないかと思います。
食品の機能性表示制度とは
4月から食品の機能性表示制度が始まりました。安全性と機能性の根拠となる科学的データがあれば、消費者庁に届け出ることで“事業者の責任において”、食品の機能性に関して表示ができるようになるこの制度。機能性表示食品は、早いもので6月ごろから店頭に並ぶことになります。
<新制度のポイント>
1.トクホとは異なり、国が安全性と機能性の審査を行いません。科学的根拠の内容・説明、科学的根拠と表示内容に乖離(かいり)がないことなどは、事業者の責任となります。
2.消費者庁に販売日の60日前までに届け出なければなりません。届け出た資料は、一部を除き消費者庁のサイトで全て開示され、他の事業者や消費者が内容を確認できます。
3.生鮮食品を含め、全ての食品が対象※となります。従って、食品・飲料メーカーだけでなく、機能性素材メーカー、商社、農家などさまざまな業種の参入が予想されます。
※アルコールを含む飲料、脂質やナトリウムの過剰摂取につながる食品などは対象外になります。
<機能性表示のポイント>
健康の維持・増進にどのような効果があるかを表示できます。
例えば、「目の健康を維持する」「良質な睡眠をサポートする」など、体の特定の部位の表示も可能。「糖尿病の人に」「高血圧の人向けに」といった、疾病の治療・予防効果を暗示する表現や、「増毛」「美白」といった、健康の維持・増進の範囲を超えた表現はできません。
電通ヘルスケアチーム
生活者視点とクリエーティビティーを強みに、「健康先進国日本」の実現とそれに向けた企業サポート業務を行っています。重要テーマの一つ「食品の機能性表示制度」については、さらに専門チームを立ち上げ、関連企業のコンサルティングやコミュニケーション業務などのサービスを提供しています。



